Los fertilizantes líquidos ofrecen ventajas como una absorción rápida y una distribución homogénea en los cultivos. Sin embargo, su formulación requiere comprender las reacciones químicas involucradas para evitar inestabilidades y problemas de compatibilidad.
Principales reacciones en fertilizantes líquidos
- Neutralización de ácidos y bases
- Se usa para ajustar el pH y mejorar la solubilidad de los nutrientes.
- Ejemplo: Neutralización del ácido fosfórico con hidóxido de potasio:
- Reacciones de quelación
- Permiten estabilizar micronutrientes en solución.
- Ejemplo: Quelación del hierro con EDTA:
- Solubilización de compuestos
- Garantiza la disponibilidad de los nutrientes esenciales.
- Ejemplo: Disolución del nitrato de calcio en agua:
- Reacciones de oxidación y reducción (redox)
- Determinan la estabilidad de elementos como hierro y manganeso.
- Ejemplo: Oxidación del hierro ferroso (Fe²⁺) a hierro férrico (Fe³⁺):
Buenas prácticas en la formulación
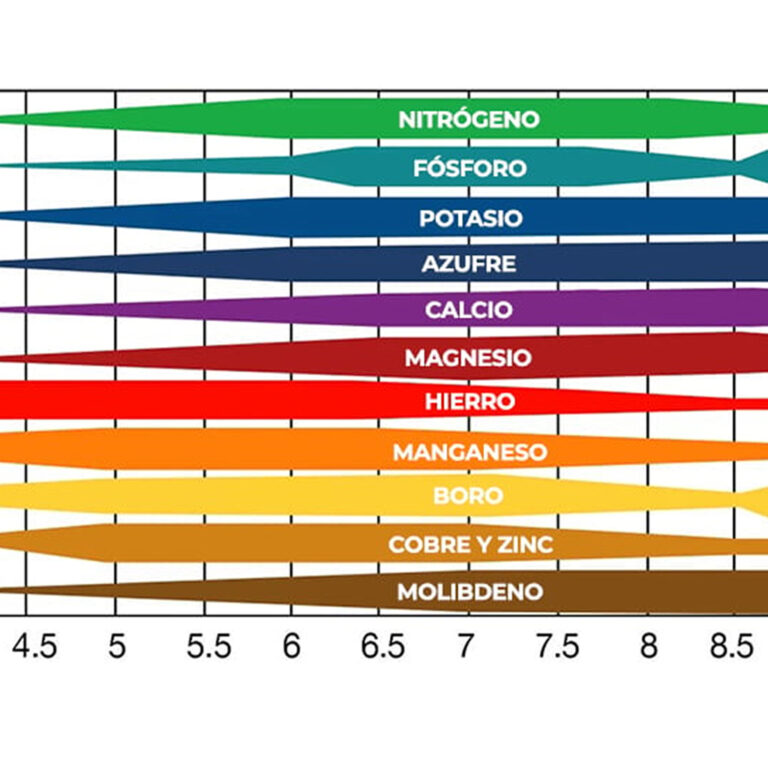
- Control de pH: Ajustar el pH según el tipo de fertilizante para evitar reacciones adversas.
- Evitar incompatibilidades: No mezclar nutrientes que puedan precipitarse.
- Uso de estabilizadores: Incorporar reguladores de pH o agentes quelantes.
- Pruebas de compatibilidad: Realizar ensayos a pequeña escala antes de aplicar en producción masiva.
Conclusión
El conocimiento de las reacciones químicas en fertilizantes líquidos permite desarrollar soluciones más estables y efectivas. Controlar el pH, evitar interacciones perjudiciales y optimizar la solubilidad garantiza una nutrición eficiente y sostenible para los cultivos.